犬の粘液腫性僧帽弁疾患
犬の粘液腫性僧帽弁疾患 について
最終更新日 : 2026年2月16日
犬の粘液腫性僧帽弁疾患
【救急チェック】心臓の悲鳴を見逃さないでください
※以下の症状がある場合、一刻を争う「肺水腫」の可能性があります
- 1. 咳が出る:特に夜間や明け方、興奮時に「カッカッ」と乾いた咳をする。
- 2. 呼吸が速い:安静時や寝ている時に、1分間の呼吸数が30回を超えている。
- 3. 舌が紫・白い:酸素が足りず、チアノーゼを起こしている。
- 4. ぐったりしている:散歩を嫌がる、すぐに座り込んでしまう。
深夜・早朝を問わず、おかしいと感じたら今すぐお電話ください。
犬の心臓病の中で最も多く、特にチワワやトイプードルなどの小型犬で頻繁に見られるのが「僧帽弁閉鎖不全症(粘液腫性僧帽弁疾患:MMVD)」です。
当院は1989年の開業以来、37年にわたり数多くの心臓病患者と向き合ってきました。当院では、世界で最も信頼されているACVIM(米国獣医内科学会)の最新コンセンサスガイドラインに基づき、根拠のある診断と治療を行っています。
1. ACVIMガイドラインに基づく「病期(ステージ)」
心臓の状態を正しく把握するため、当院では以下のステージ分類を用いて治療方針を決定します。どの段階で適切な介入を始めるかが、寿命を左右します。
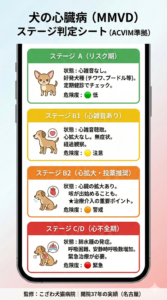
| ステージ | 状態の詳細 | 当院の対応 |
|---|---|---|
| ステージ A | 心臓病のリスクがある犬種(健康) | 定期的な心雑音のチェック |
| ステージ B1 | 心雑音はあるが、心肥大は見られない | レントゲン・エコーでの経過観察 |
| ステージ B2 | 心肥大が認められる(投薬開始時期) | ★最新薬による寿命延長の開始 |
| ステージ C | 心不全(肺水腫)を起こしたことがある | 強力な利尿剤・強心剤による管理 |
| ステージ D | 通常の治療に反応しない末期状態 | 高度な集中治療・緩和ケア |
こざわ犬猫病院が「心臓の救急」に選ばれる理由
- 1. 37年の圧倒的な臨床経験:1989年の開業以来、数えきれないほどの心臓病治療に携わってきた実績があります。
- 2. 深夜〜朝9時の救急対応:心不全による呼吸困難は、夜間に起こることが非常に多いです。当院は365日、深夜でも即座に酸素療法や緊急処置を行える体制を整えています。
- 3. 飼い主様に寄り添う治療選択:内科的な維持療法から、生活の質(QOL)を最優先したケアまで、ご家族としっかり対話して決定します。
【保存版】愛犬の心臓を守る「安静時呼吸数(SRR)」の測り方
僧帽弁閉鎖不全症において、肺に水が溜まる「肺水腫」の兆候を最も早く見つける方法が、寝ている時の呼吸数を数えることです。
測り方のステップ:
- ワンちゃんが「深く寝ている時」に測ります(※動いている時は正確に測れません)。
- 胸やお腹が「1回膨らんで、1回へこむ」のを「1回」と数えます。
- 1分間数えます。(※30秒間数えて2倍してもOKです)
判定の目安(1分間あたり):
| 30回未満 | 正常。 落ち着いています。今のペースを維持しましょう。 |
|---|---|
| 30〜40回 | 注意。 少し速めです。数時間後に再測定し、続くようなら受診を検討。 |
| 40回以上 | 緊急! 肺水腫の疑いがあります。深夜・早朝を問わず直ちにお電話ください。 |
安静時呼吸数(SRR)チェック表
日々の変化を記録して、次回の診察時にお持ちください。スマホでこの表をスクリーンショットして記録するのもおすすめです。
2. 治療において最も大切なこと僧帽弁閉鎖不全症の治療のゴールは、単に心臓の音を良くすることではなく、「愛犬がいかに苦しまず、ご家族と長く一緒に過ごせるか」にあります。早期発見ができれば、最新のガイドラインに基づいた投薬によって、心不全の発症を大幅に遅らせることが可能です。もし「最近咳が増えた」「呼吸が荒い気がする」と感じたら、一人で悩まずに当院へご相談ください。37年の経験に基づき、全力でサポートさせていただきます。
https://www.anicare.net/urgent/
| 日付 | 呼吸数(/分) | メモ(咳の有無など) |
|---|



